相平衡理论--二元系(2)
- 发布人:管理员
- 发布时间:2014-04-18
- 浏览量:792
MgO-CaO二元系
MgO-CaO二元系相平衡状态图如图5所示。
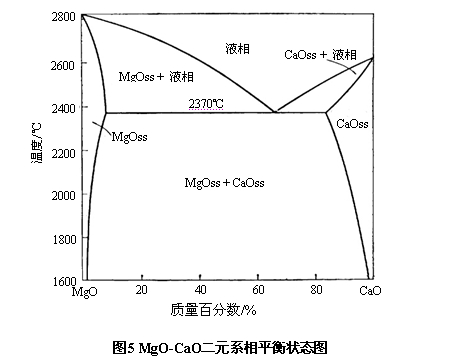
由图可知,MgO和CaO两种氧化物的二元系统中无二元化合物。共熔温度很高,达2370℃。因此,由纯MgO和CaO构成的耐火材料在2370℃以下不会出现液相,从而使其具有高的耐火度。
CaO和MgO共存时,在高温下具有一定的互溶性,而且其溶解度随温度的升高而增大。CaO在MgO中的溶解度可由1620℃时的0.9%增加到2370℃时的7.8%。MgO在CaO中的溶解度则由1620℃时的2.5%增加到2370℃时的17%。因此,在镁质耐火材料中,若有硅酸盐存在并与MgO接触时,则MgO也可从硅酸盐中夺取CaO以生成MgO-CaO固溶体。一般来说,硅酸盐中的CaO/SiO2值越大,被夺走的CaO数量越多,从而影响系统中的CaO/SiO2值,因此,MgO与CaO组分间的互溶,会引起材料中相组成的相应变化,进而促进材料的烧结并影响材料的性能。
MgO·Al2O3-2CaO·SiO2二元系
MgO·Al2O3-2CaO·SiO2二元系相平衡状态图如图6所示。
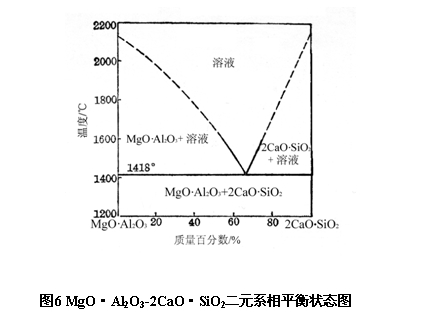
由图可见,在此体系内有一共熔点,其温度为1418℃,成分为MgO·Al2O3:35%,CaO·SiO2:65%。因此,对于尖晶石系耐火材料来说,随着其中硅酸盐浸入量的增加,其耐火度会明显下降。
MgO·Al2O3-CaO·MgO·SiO2二元系
MgO·Al2O3-CaO·MgO·SiO2假二元系相平衡状态图如图7所示。

在此二元体系内,CaO·MgO·SiO2相为分解熔融,而且其分解温度不变。因此,当尖晶石系耐火材料与CaO-SiO2系熔渣接触时,即使MgO组分熔入CaO-SiO2体系内,虽然可以改变CaO-SiO2体系的粘度,但对于耐火材料的熔点是没有影响的。
MgO·Al2O3-2MgO·SiO2二元系
MgO·Al2O3-2MgO·SiO2二元系相平衡状态图如图8所示。
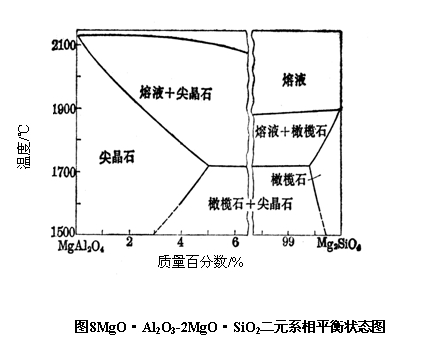
MgO·Al2O3与2MgO·SiO2均可以互溶,但2MgO·SiO2溶于MgO·Al2O3中的量要大于MgO·Al2O3溶于2MgO·SiO2 中的量。最大固溶量在其共熔点温度,即,1700℃。
上一篇:相平衡理论--二元系(1)





